Coordenadora:
Dra. Marcia Motta Maués • Embrapa Amazônia Oriental (e-mail: marcia.maues@embrapa.br)
Pesquisadores responsáveis:
Amapá - Dr. Alexandre Luis Jordão (IEPA);
Dr. Carlos Alberto Hector Flechtmann (UNESP - Ilha Solteira/SP) - Colaborador
Leste do Pará - Dr. Hermes Fonseca de Medeiros (UFPA)
Maranhão - Dr. Francisco Limeira de Oliveira (UEMA)
Mato Grosso - Dr. Evandson José dos Anjos Silva (UNEMAT-Cárceres)
Oeste do Pará - M.Sc. Yukari Okada (UFOPA)
Grupos de interesse e diversidade de espécies estimada por sítio de coleta:
Apidae - 120 espécies.
Drosophilidae - 40 espécies;
Mesembrinellidae - 10 espécies;
Nymphalidae - 40 espécies;
Tephritidae - 15 espécies;
Scolytinae e Platypodinae (Curculionidae) - 100 espécies.
Papel biológico do grupo:
As abelhas são insetos pertencentes à ordem Hymenoptera e família Apidae, com estimativas de que existam no mundo cerca de 30.000 espécies. Além de constituírem um dos grupos mais ricos em espécies na região neotropical, contribuem também para a diversidade dos organismos com os quais se relacionam, através da polinização cruzada. Entre seus papéis, destacam-se os de polinizadores de um grande número de espécies vegetais, tanto nativos quanto cultivados (OLIVEIRA; MORATO, 2000; GREENLEAF; KREMEN, 2006), dispersores de frutos e provavelmente dispersores de esporos de fungos (ELTZ et al., 2002). Além disso, muitas espécies têm seus produtos, sobretudo mel e cera, utilizados na alimentação, farmacopeia e complemento da renda familiar.
As moscas estão inseridas na ordem Diptera, que é composta de 45 famílias, sendo que destas, Y famílias são conhecidas vulgarmente como moscas. As moscas que utilizam matéria orgânica vegetal em decomposição para alimentação e reprodução desempenham importante papel como organismos saprófagos, atuando nos processos de decomposição e ciclagem de nutrientes. Algumas destas também podem utilizar frutos maduros, atuando como herbívoros, podendo alcançar grande importância econômica, como pragas em ambientes agrícolas (TIDON et al., 2003). No entanto, várias espécies podem também desempenhar o papel de polinizadores, quando na utilização de flores como substrato de alimentação e oviposição (SILVA; MARTINS, 2003).Pode-se encontrar vários graus de associações das moscas com o homem, desde uma associação total até espécies que ocorrem apenas em ambientes pristinos. Essa sensibilidade em relação aos ambientes, aliada à rapidez de resposta em termos populacionais, confere às moscas a capacidade de funcionarem como indicadores de interferências humanas nos ambientes naturais (MARTINS, 2001).
As borboletas são representadas por cinco famílias: Hesperiidae, Papilionidae, Pieridae, Lycaenidae, e Nymphalidae. As formas adultas apresentam hábitos diurnos e alimentam-se de matéria em decomposição, exsudados de plantas e néctar. As borboletas que se alimentam de frutas em fermentação compõem mais ou menos um terço das espécies de borboletas numa floresta neotropical. Estas borboletas pertencem à família Nymphalidae, e é o único grupo de borboletas que pode ser levantado através de armadilhas. Taxonomicamente, o grupo é bem conhecido e pode ser utilizado em levantamentos, avaliações ecológicas rápidas e monitoramento. Devido à sua relação íntima com a vegetação durante as suas fases larval e adulta, as borboletas candidatam-se como bioindicadores de mudanças ambientais (FREITAS, 2008). O inventário da fauna de borboletas frugívoras é essencial para que entendimento da comunidade, bem como para desenvolver mecanismos para sua preservação (FERRO; DINIZ, 2007).
Besouros das sub-famílias Scolytinae e Platypodinae (Curculionidae) são tipicamente brocas de árvores e arbustos. Dentro destes grupos encontram-se as espécies mais evoluídas da família Curculionidae, havendo várias que cultivam o próprio alimento, com algumas outras ainda mostrando um cuidado maternal. Estas brocas são um grupo bastante grande, com mais de 7000 espécies descritas, e são encontradas tipicamente em ambiente florestal. Em florestas naturais estes besouros desempenham papel bastante importante na reciclagem de nutrientes, ao atacarem e se desenvolverem em plantas hospedeiras estressadas e/ou à morte. Já em florestas implantadas, constituem-se em pragas muito sérias, podendo estar entre os maiores causadores de danos de ordem biológica (Wood 2007). Além da importância ecológica que estes besouros possuem em ambientes naturais e a importância econômica principalmente em florestas implantadas, estes organismos possuem ainda uma importância muito grande como bioindicadores de preservação e degradação ambiental. Há várias espécies conhecidas como de interior, e estas encontram-se geralmente presentes somente em áreas muito bem preservadas. Em contrapartida, há espécies denominadas como de borda, cuja presença indica áreas antropizadas ou perturbadas. Desta forma, estes besouros prestam-se como excelentes indicadores do estado de conservação de um habitat.
Metodologias aplicadas:
A) TÉCNICA 1 - ARMADILHAS PARA MOSCAS (DIPTERA) COM ISCAS DE BANANA
As iscas de banana são usadas nas armadilhas apresentadas na Figura 1. A isca é preparada com bananas maduras, amassadas até obter-se uma massa homogênea no dia anterior à coleta. Cada armadilha recebe em torno de 100 ml de isca, e é pendurada a aproximadamente 30 cm do solo, permanecendo no campo por 48 horas. Após este período, os animais retidos nas armadilhas são coletados com o uso de um aspirador manual.
Este método é direcionado primariamente para moscas da família Drosophilidae, mas captura dois dos grupos-alvo: Drosophilidae e Mesembrinellidae.

Figura 1- Armadilha para isca de banana.
B) TÉCNICA 2 - ARMADILHAS PARA MOSCAS (DIPTERA) COM ISCAS DE MELADO
As iscas de melado são usadas nas armadilhas apresentadas na Figura 2. A isca consiste em solução aquosa contendo 10% de melado e 1% de bórax. A isca deve ser preparada no mesmo dia da colocação das armadilhas no campo. Cada armadilha recebe em torno de 150 ml de isca e é pendurada a aproximadamente 150 cm do solo, permanecendo no campo por 48 horas. Após este período, a isca é derramada em uma peneira fina, para que sejam coletados os animais que caíram no líquido. Este método é direcionado primariamente para mosca-das-frutas (família Tephritidae), mas também abrange os mesmos grupos citados na TÉCNICA 1.
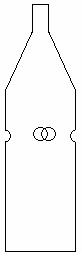
Figura 2- Armadilha para isca melado de cana. Consiste simplesmente em uma garrafa plástica de 2 litros, na qual foram feitos quatro buracos de 2 centímetros de diâmetro. A solução com melado de cana é depositada no fundo da garrafa.
C) TÉCNICA 3 - ARMADILHAS PARA MOSCAS COM ISCAS DE PROTEÍNA
Serão utilizadas armadilhas confeccionadas artesanalmente a partir de garrafas pet de 1,5 L, com quatro orifícios de 2 cm, diametralmente opostos, contendo 300 ml de proteína hidrolisada e estabilizada a 5% com bórax em cada armadilha. Também serão utilizadas armadilhas com isca de pulmão (Figura 3). Esta armadilha é composta de uma lata de 500 gramas recoberta por um saco plástico transparente. As latas possuem perfurações laterais por onde as moscas entram e um funil de papel invertido é colocado sobre a lata, no acesso da lata para o saco plástico, que recobre a parte superior. As armadilhas dessa técnica serão distribuídas em 30 parcelas com o espaçamento regular de 40 metros entre elas recebendo, cada parcela, três armadilhas, sendo as mesmas penduradas a 1,80 m do solo, gerando com isso um total de 90 amostras. As amostras serão colocadas em frascos com álcool a 70%, os quais serão etiquetados, contendo o número da armadilha, local e a data de inspeção.

Figura 3- Armadilha para isca de pulmão.
D) TÉCNICA 4 - ARMADILHAS COM ISCAS PARA ABELHAS DAS ORQUÍDEAS (EUGLOSSINI)
A isca consiste em essências, colocadas no algodão da armadilha na hora de colocar a armadilha no campo (NEMÉSIO; SILVEIRA, 2006). O volume da essência colocada no algodão depende do tipo de essência empregado, pois elas diferem no poder de atração (CARVALHO et al., 2006; ZIMMERMANN et al., 2006). A isca a ser utilizada é o salicilato de metila. Outros atrativos que poderão ser usados são: cineol, vanilina e cinamato de metila.
Para a aplicação de um desenho amostral amplo é necessário que a isca mantenha uma atratividade constante durante um período de mais de 24 horas, para que o efeito espacial não seja confundido com o efeito da variação circadiana na atividade dos animais. Isto foi obtido em uma coleta de avaliação do protocolo com o uso de 2 ml de salicilato de metila. O uso dos outros atrativos pode ser feito sem seguir o desenho amostral descrito abaixo, como uma complementação de amostragem, visando basicamente à ampliação da lista de espécies obtidas.
Cada armadilha é pendurada a aproximadamente 1,5 m do solo (Figura 4), permanecendo no campo por 24 horas. Após este período, a armadilha é fechada e são removidas as abelhas retidas. Para a retirada das abelhas, pode-se apenas fechar as entradas das armadilhas e esperar que os animais retidos morram intoxicados pela própria isca; ou inserir na armadilha alguma substância para sacrificá-los. No segundo caso, é necessário se certificar de que a substância empregada não deixou resíduos, antes de utilizar as mesmas armadilhas novamente.

Figura 4. Armadilha para abelhas Euglossini. Em cada um de três furos é inserido um funil feito com um gargalo de garrafa plástica. Este funil é recoberto internamente por areia colada com cola de isopor e são colados nos buracos. Na tampa da garrafa é inserido um palito de churrasco, no qual é preso um chumaço de algodão, no qual é colocada a isca.
• Unidade amostral: O resultado de uma armadilha em um período de coleta.
• Desenho amostral: Todas as 30 parcelas receberão igual número de armadilhas. Para as técnicas 1, 2 e 3 serão dispostas 4 armadilhas de cada tipo por parcela. A técnica 1 é empregada juntamente com a técnica de coleta 2, mantendo uma distribuição regular e intercalando os dois métodos. As outras duas técnicas são colocadas juntas, sendo que as armadilhas de Euglossini são colocadas a 200 metros uma da outra.
• Dados ambientais adicionais importantes para o grupo: Dados microclimáticos de temperatura, luz, precipitação e umidade são importantes para os grupos-alvo deste protocolo. Microestações meteorológicas podem ser utilizadas para a obtenção destes dados. Cada parcela será monitorada por 48 horas, coincidindo com o tempo de exposição das armadilhas, com três microestações, distribuídas aleatoriamente dentro da parcela.
• Forma de preservação do material coletado: O material proveniente das armadilhas de banana e melado de cana será preservado em álcool a 70% e, posteriormente, até 10 casais de cada espécie determinada. No caso dos drosofilídeos, alguns exemplares serão mantidos vivos em estoques de isofêmeas para facilitar a identificação taxonômica e tornar-se-ão também disponíveis para outros estudos (DAVID et. al., 2005). As abelhas das orquídeas que não estiverem mortas na hora de se recolher as armadilhas serão sacrificadas e depois guardadas em envelopes (tipo pipoca), com as anotações necessárias. Os exemplares serão acondicionados em marmitas de alumínio, contendo algumas gotas de acetato de etila para evitar ataque de fungos ou apodrecimento. No laboratório serão montadas em alfinete entomológico, etiquetadas e identificadas. Todas as unicatas e espécimes não identificados ficarão nas respectivas instituições dos especialistas e os demais comporão coleções de referência em todas as instituições participantes do PPBio interessadas, desde que haja condições mínimas de conservação do material.Tanto o material em álcool quanto montado será depositado nas coleções cientificas das instituições envolvidas.
E) TÉCNICA 5 - ARMADILHA COM ISCA DE FRUTAS PARA BORBOLETAS
Cada armadilha consiste de um cilindro de uma tela de pano fechado (náilon) no topo, com uma armação de metal no topo e no fundo. A tela de pano apresenta uma abertura vertical de 50 cm, que corre ao longo de seu comprimento e que é fechada com velcro, pela qual as borboletas podem ser retiradas da armadilha. Suspenso no anel da parte inferior do cilindro há um pedaço quadrado de madeira pendurado a cerca de 5 cm abaixo da abertura do cilindro. Sobre o quadrado de compensado será colocado um pequeno recipiente plástico, com uma pasta de banana amassada e fermentada durante mais de 48 horas, na base do compensado, como a isca para atrair as borboletas. Uma descrição detalhada da armadilha pode ser obtida em DeVries (1988).
A isca de banana é preparada com bananas maduras, amassadas até obter-se uma massa homogênea, pelo menos três dias antes da coleta. A fermentação é natural, ou seja, sem adição às bananas de fermento biológico. Cada armadilha recebe em torno de 100 ml de isca.
No sub-bosque, as armadilhas serão penduradas a 1,0 a 1,5 m acima do chão, utilizando-se uma corda para sustentá-la em um galhos baixos. A vegetação não é cortada ou modificada para a colocação das armadilhas. A coleta em cada parcela será de 5 dias consecutivos. As armadilhas serão visitadas cada dia e a isca renovada no terceiro dia. As borboletas são removidas com uso de pinças a cada 24 horas.
• Unidade amostral: O resultado de uma armadilha em um período de 24 horas.
• Desenho amostral: Em cada parcela serão colocadas 6 armadilhas, distribuídas ao longo da trilha principal de cada parcela a intervalos de 50 m (0 m, 50 m, ... 250 m). As armadilhas serão colocadas a não mais de 5 m da trilha. A coleta em 30 parcelas levará 15 dias, uma vez que a equipe pode atender a 10 parcelas em cada 5 dias. As armadilhas serão deslocadas para a coleta e guardadas entre as excursões. São previstas quatro coletas por ano, duas na época seca e duas na época chuvosa.
• Tratamento do material: O material proveniente das armadilhas de banana será sacrificado em frasco mortífero contendo Acetato de Etila, e guardados em envelopes entomológicos com as anotações necessárias e acondicionados em marmitas plásticas contendo naftalina para evitar ataque de fungos ou apodrecimento. No laboratório serão montadas em alfinete entomológico, etiquetadas e identificadas. Todas as unicatas e espécimes não identificados ficam nas respectivas instituições dos especialistas e os demais comporão coleções de referência em todas as instituições participantes do PPBio interessadas, desde que haja condições mínimas de conservação do material.

Figura 5. Armadilha para borboletas frugívoras. Confeccionadas de filo, com base de madeira. São cilíndricas, medindo 70. A entrada para as borboletas é a abertura entre a base e o cilíndrico de filo, medindo 3 cm em altura, onde é colocado um prato com isca de banana fermentada.
F) TÉCNICA 6 - ARMADILHA PARA SCOLYTINAE/PLATYPODINAE (CURCULIONIDAE)
Para a coleta destas brocas, utiliza-se de armadilhas de impacto de vôo (BERTI Filho & FLECHTMANN, 1986). Esta armadilha pode também ser facilmente confeccionada utilizando-se de garrafas PET transparentes de refrigerante de 2 litros (Figura 7).

Figura 6 - Armadilha de impacto de vôo ESALQ-84.

Figura 7 - Armadilha de impacto de vôo ESALQ-84 modificada, usando de garrafa PET.
Estas armadilhas são iscadas com etanol comercial, que é o semioquímico mais utilizado no Brasil (FLECHTMANN et al., 2001). O etanol é colocado em frasco de penicilina cuja tampa é trespassada por um tubo para infusão venosa de cerca de 3 mm de diâmetro. No interior do tubo passa-se uma corda, pelo qual o etanol, por capilaridade, é volatilizado ao meio externo numa taxa constante de liberação.

Figura 8 - Recipiente com etanol 95% como isca atrativa.
Cada armadilha é dependurada a 1,50 m do solo, tomando-se como referência na armadilha o frasco contendo o atrativo, o etanol. O recipiente coletor deve conter água com algumas gotas de detergente, para quebrar a tensão superficial da água, e um pouco de sal, quando necessário para auxiliar na conservação dos insetos capturados. A armadilha deve permanecer por 7 dias no campo, após o qual os insetos capturados são removidos, o líquido do recipiente coletor é substituído e o etanol é reposto quando necessário. Deve-se ter o cuidado de se manter sempre o funil limpo em sua parte interna.
. Unidade amostral: o resultado de uma armadilha em um período de coleta (7 dias).
. Desenho amostral: para uma área homogênea, são suficientes 5 armadilhas, distribuídas homogeneamente. Para áreas divididas em quadrantes, deve-se agrupar aqueles com características similares de vegetação e altitude, e colocar ao menos 5 armadilhas para cada agrupamento. Deve-se sempre posicionar as armadilhas ao menos 20 m ao interior de cada área, para evitar efeito de borda. A frequência de coleta é semanal. O ideal é que as coletas sejam feitas por um ano, para se conhecer a variação sazonal dos insetos, mas quando este não é o objetivo ou isto não é possível, fazer ao menos 15 coletas na estação chuvosa, quando estes são geralmente mais abundantes.
. Tratamento do material: insetos coletados devem ser transferidos a frascos contendo álcool 70%, e assim armazenados até sua identificação. Para cada site deverá-se montar uma série de ao menos 10 espécimes para cada morfotipo, os quais deverão ser devidamente etiquetados, com dados de coleta sempre em inglês.
. Dados ambientais adicionais importantes para o grupo: para Scolytinae/Platypodinae, é importante registrar dados diários de temperatura média do ar, umidade relativa média do ar e precipitação pluvial, obtidos da estação meteorológica mais próxima.
Restrições a atividades que prejudiquem o desenvolvimento do protocolo:
Considerando-se que a maioria dos Diptera e Hymenoptera são atraídos por material em decomposição, nenhuma deposição de detritos orgânicos de qualquer espécie deve ser permitida, incluindo-se lixo proveniente de acampamentos. Quando os organismos-alvo são Scolytinae/Platypodinae, evitar áreas onde corte de árvores ou áreas afetadas por tempestades que tenham gerado em árvores caídas.
Referências:
BERTI FILHO, E.; FLECHTMANN, C.A.H. A model of ethanol trap to collect Scolytidae and Platypodidae (Insecta, Coleoptera). IPEF, n. 34, p. 53-56, 1986.
CARVALHO, C.C.; REGO, M.M.C.; MENDES, F.M. Dinâmica de populações de Euglossina (Hymenoptera, Apidae) em mata ciliar, Urbano Santos, Maranhão, Brasil. Iheringia, Sér. Zool., vol. 96, n. 2, p.249-256. 2006.
COSTA, C. Coleoptera linnaeus, 1758. In: JOLY, C.A.; BICUDO, C. (Orgs.) Biodiversidade do Estado de São Paulo. Síntese do conhecimento ao final do século XX. São Paulo: FAPESP, 1999. p. 115-122.
DAVID, P. G.; LEGOUT, H.; PE´TAVY, G.; CAPY, P.; MORETEAU, B. Isofemale lines in Drosophila: an empirical approach to quantitative trait analysis in natural populations. Heredity, v. 94, p. 312, 2005/2006.
ELTZ, T.; BRÜHL, C.A.; GÖRKE, C. Collection of mold (Rhizopus sp.) spores in lieu of pollen by the stingless bee Trigona collina. Insectes Soc., v. 49, p. 28-30, 2002.
FLECHTMANN, C.A.H.; OTTATI, A.L.T., BERISFORD, C.W. Ambrosia and bark beetles (Scolytidae: Coleoptera) in pine and eucalypt stands in southern Brazil. For. Ecol. Manag., v. 142, n. 1/3, p. 183-191, 2001.
MARTINS, M.B. Guilds of Drosophilids on Forest Fragments. In: BIERREGAARD, R.O.; GASCON, C.; LOVEJOY, T.E. (Orgs.). Lessons from Amazonia. The ecology and conservation of a fragmented forest. Yale: yale University, 2001.
OLIVEIRA, M.L.; MORATO, E.F. Stingless bees (Hymenoptera, Meliponini) feeding on stinkhorn spores (Fungi, Phallales): robbery or dispersal? Revta. Bras. Zool., v.17, p. 881-884, 2000.
GREENLEAF, S.S.; KREMEN, C. Wild bee species increase tomato production and respond differently to surrounding land use in Northern Califórnia. Biological Conservation, v.133, n. 1, p. 81-87, 2006.
NEMÉSIO, A.; SILVEIRA, F.A. Edge Effects on the Orchid-Bee Fauna (Hymenoptera: Apidae) at a Large Remnant of Atlantic Rain Forest in Southeastern Brazil. Neotropical Entomology, v. 35, n. 3, p. 313-323, 2006.
SILVA, A.R.; MARTINS, M.B. Insetos polinizadores de Theobroma speciosum (Sterculiaceae) e conservação da biodiversidade. In: Estação Científica Ferreira Penna - dez anos de pesquisa na Amazônia; contribuições e novos desafios. Belém: MPEG, 2003. (Cadernos e Debates, v. 7).
TIDON, R.; LEITE, D.F.; LEÃO, B.F.D. Impact of the colonisation of Zaprionus (Dipetra, Drosophilidae) in different ecosystems of Neotropical Region: 2 years after the invasion. Biological Conservation, v. 112, p.299-305, 2003.
WOOD, S.L. Bark and ambrosia beetles of South America (Coleoptera: Scolytidae). Brigham Young University, Provo. 900 pp., 2007.
ZIMMERMANN, Y.; ROUBIK, W.D.; ELTZ, T. Species-specific attraction to pheromonal analogues in orchid bees. Behav Ecol. Sociobiol, v. 60, p. 833-843, 2006.